Сухожилия это суспензия эмульсия
Содержание статьи
Дисперсные системы. Способы выражения состава растворов
ДИСПЕРСНЫЕ СИСТЕМЫ. ИСТИННЫЕ РАСТВОРЫ
Чистые вещества встречаются достаточно редко. Строго говоря, абсолютно чистых веществ в природе не существует. Как бы мы ни старались очистить, например, воду, она будет содержать примеси других веществ, в частности растворенных в ней газов. Сверхчистый кремний применяют в электронной технике, его удается очистить до невероятной степени чистоты: 99,9999999999 % основного вещества. Однако 1,0 10-10% все же приходится на примеси.
Дисперсными системами называют гетерогенные смеси, в которых одно вещество в виде очень мелких частиц равномерно распределено в другом.
Вещество, которое распределено в объеме другого, называют дисперсной фазой.Вещество, в котором содержится дисперсная фаза, носит название дисперсионной среды.
В зависимости от агрегатного состояния дисперсной фазы и дисперсионной среды различают несколько типов дисперсных систем (табл.).
По размеру частиц дисперсной фазы различают грубодисперсные системы(взвеси) с частицами размером более 100 нм итонкодисперсные(коллоидные системы,или коллоиды) с частицами размером от 1 до 100 нм.
Дисперсионная среда
Дисперсная фаза
Название дисперсной системы
Примеры дисперсных систем
Газ
Жидкость
Аэрозоль
Туман, облака, облачко, выпущенное из аэрозольного баллончика
Твердое
вещество
Аэрозоль
Дым, смог, пыль в воздухе
Жидкость
Газ
Пена
Газированные напитки, взбитые сливки
Жидкость
Эмульсия
Молоко, майонез, жидкие средь организма (плазма крови, лимфа), жидкое содержимое клеток (цитоплазма, кариоплазма)
Твердое
вещество
Золь, суспензия
Речной и морской ил, строительные растворы, пасты
Твердое
вещество
Газ
Твердая
пена
Керамика, пенопласты, полиуретан, поролон, пористый шоколад
Жидкость
Гель
Желе, желатин, косметические (тушь, помада) и медицинские (мази, гели, линименты — жидкие мази) средства
Твердое
вещество
Твердый
золь
Горные породы, цветные стекла, некоторые сплавы
Грубодисперсные системы
Взаимодействием раствора гидроксида кальция с углекислым газом можно получить грубодисперсную систему:
Са(ОН)2 + СО2 = CaCО3 + Н2О
Малорастворимый карбонат кальция в виде мельчайших крупинок находится в воде во взвешенном состоянии. Полученная мутная жидкость — это дисперсная система, называемая суспензией.
Однако пройдет немного времени, и частицы карбоната кальция под действием силы тяжести осядут на дно стакана, жидкость станет прозрачной. Это веское доказательство того, что наша система получилась грубодисперсной. Грубодисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой называют суспензиями.
Суспензиями являются многие краски, побелка, строительные растворы (цементный раствор, бетон), пасты (в том числе зубная), кремы, мази. Грубодисперсную систему можно получить из двух несмешивающихся друг с другом жидкостей, подобно тому, как взбалтывают растительное масло с водой. Такую смесь называют эмульсией. Со временем она расслоится, так как тоже представляет собой грубодисперсную систему. Примерами эмульсий могут служить молоко (капельки жира в водной основе), майонез, млечный сок каучуконосных деревьев (латекс), пестицидные препараты для обработки посевов, некоторые лекарственные и косметические средства.
Коллоидные системы
Если частицы дисперсной фазы достаточно малы, коллоидная система называется тонкодисперсной и напоминает истинный раствор, отсюда и происходит название — коллоидный раствор. Такая система образуется, например, при растворении небольшого количества яичного белка в воде. Важнейшими типами коллоидных систем являются золи и гели (студни).
Золи — это коллоидные системы, в которых дисперсионной средой является жидкость, дисперсной фазой твердое вещество. С течением времени при нагревании или под действием электролитов частицы золя могут укрупняться и оседать. Такой процесс называют коагуляцией.
Гели — особое студнеобразное коллоидное состояние. При этом отдельные частицы золя связываются друг с другом, образуя сплошную пространственную сетку. Внутрь ячеек сетки попадают частицы растворителя. Дисперсная система теряет свою текучесть, превращаясь в желеобразное состояние. При нагревании гель может превратиться в золь.
Получить гель можно химическим путем. К раствору сульфата меди (II) добавьте несколько капель раствора гидроксида натрия. Образуется гель осадка гидроксида меди(П):
CuSО4 + 2NaOH = Cu(OH)2 + Na2SО4
Осадки гидроксидов металлов, кремниевой кислоты принято называть студневидными.
Гели широко распространены в нашей повседневной жизни. Любому известны пищевые гели (зефир, мармелад, холодец), косметические (гель для душа), медицинские. Однако немногие знают, что хрящи, сухожилия, волосы представляют собой биологические гели, а опал, сердолик, халцедон — минеральные.
Для гелей с жидкой дисперсионной средой характерно явление синерезиса (или расслоения) — самопроизвольного выделения жидкости. При этом частицы дисперсной фазы уплотняются, слипаются и образуют твердый коллоид, а к дисперсионная среде возвращается текучесть.
Чаще всего с явлением синерезиса приходится бороться, поскольку именно оно ограничивает сроки годности пищевых, косметических, медицинских гелей. Например, при длительном хранении мармелад и суфле выделяют жидкость, становятся непригодными к употреблению. Однако в некоторых случаях синерезис — великое благо. Благодаря биологическому синерезису мы наблюдаем такое явление, как свертывание крови, суть которого состоит в превращении растворимого белка фибриногена в нерастворимый фибрин.
Из твердого коллоида желатины (продукта белкового происхождения) при набухании в теплой воде образуется студнеобразный гель — желе. Но в кулинарных рецептах всегда предупреждают: нельзя доводить желе до кипения, иначе гель превратится в золь и не примет своей студнеобразной формы.
Окружающий нас мир представляет собой многообразие различных дисперсных систем. Посмотрим вокруг. Косметика и средства гигиены: зубная паста, мыло, шампунь, лак для ногтей, губная помада, тушь, крем, облачка дезодоранта, выпущенное из баллончика, — все это дисперсные системы. Теперь заглянем на кухню. Молоко, мясной бульон, пирожное, зефир, майонез, кетчуп — тоже представляют собой разнообразные дисперсные системы. Вышли на улицу, и снова окунулись в мир дисперсных систем: облака, дым, смог, туман. Заглянули в аптеку и опять попали в калейдоскоп дисперсных систем: мази, гели, пасты, спреи, сусспензии. Даже собственный организм представляет собой сочетание бесчисленного множества коллоидных систем: содержимое клетки, кровь, лимфа, пищеварительный сок, тканевые жидкости. Недаром биологи сходятся во мнении, что жизнь на на! шей планете представляет собой эволюцию коллоидных систем.
Истинные растворы
Помимо коллоидных существуют растворы истинные. В них растворенное вещество присутствует в виде самых маленьких частиц, на которое оно способно распадаться: молекул или ионов – раствораминазывают гомогенные (однородные) смеси, состоящие из двух или более компонентов.
Наиболее важную роль в природе, технике, производстве, в повседневной жизни играют растворы веществ в воде.
Как правило, если одним из компонентов раствора является вода, ее и называют растворителем, остальные компоненты растворенными веществами.
Растворимость в воде газообразных веществ существенно различается. Например, кислород, водород, азот, углекислый газ растворяются плохо, поэтому их можно собирать в сосуд метолом вытеснения воды. Тем не менее именно растворенным в воде кислородом дышат все водные обитатели. Газообразный хлороводород хорошо растворим в воде, такой раствор называют соляной кислотой. Примером хорошо растворимого в воде газа может служить аммиак (его раствор называют водным аммиаком, или нашатырным спиртом).
Бензин, растительное масло, ртуть в воде практически не растворяются. Серная кислота, уксусная кислота, ацетон — примеры жидкостей, которые в воде растворяются неограниченно.
Среди твердых веществ также есть практически нерастворимые: это хлорид серебра(I), оксид кремния(IV), золото. Напротив, сахар, поваренная соль, нитрат серебра(I) в воде растворяются хорошо.
Растворимость веществ зависит от природы вещества и растворителя, температуры, давления (для газообразных веществ) и других факторов.
При увеличении температуры растворимость газов уменьшается. Это легко обнаружить при нагревании воды в кастрюле: по мере увеличения температуры (еще ниже температуры кипения) на стенках появляются маленькие пузырьки воздуха. Чтобы удалить из воды значительную часть растворенных газов, ее кипятят. Растворимость в воде жидкостей и твердых веществ с повышением температуры, как правило, увеличивается.
Чем больше давление, тем выше растворимость газов в воде. Каждый знает, что при открывании бутылки или банки с газированным напитком давление внутри резко падает, и углекислый газ в виде пузырьков, а порой и пены вырывается из раствора на свободу.
Содержание растворенного вещества в растворе называют концентрацией. Помимо качественной оценки (концентрированный или разбавленный растворы) существуют строгие количественные характеристики.
На этикетках разнообразных растворов, используемых в быту можно прочитать указание на содержание растворенного вещества; например, уксусная кислота 70 %, настойка иода 5 %, нашатырный спирт 25 %. Это один из самых распространенных способов выражения концентрации растворов, который называют массовой долей растворенного вещества.
Массовой долей вещества в растворе (ω) называют отношение массы растворенного вещества (mp.в) к массе растора (mp-ра):
%
Массовую долю вещества выражают в процентах (от 0 до 100 % или долях единицы (от 0 до 1).
Очевидно, что масса раствора складывается из массы растворителя и массы всех растворенных веществ. Если растворенное вещество только одно, то справедливо уравнение
m(раствора) = m(вещество) + m(растворитель).
Отмерять жидкости взвешиванием не очень удобно, гораздо проще брать нужный объем. Чтобы рассчитать массу т известно го объема V раствора, необходимо знать его плотность ρ:
m(раствора) = V (раствора)•ρ
Источник
Эмульсии и суспензии
К жидким лекарственным формам относятся растворы, слизи, эмульсии, суспензии, настои и отвары, настойки, жидкие экстракты, микстуры. В рамках данной статьи будет произведен обзор суспензии и эмульсий + разницы между ними. Такое большое разнообразие жидких форм создает некие сложности в классификации и понимании.
У многих людей возникает закономерный и логичный вопрос — чем отличаются друг от друга суспензии и эмульсии. В данной статье мы разберем суспензии и эмульсии, как лекарственные формы, но это сравнение применительно и в быту, и в пищевой промышленности.мы обратимся к официальным государственным фармакопеям, и на основе этих определений будем строить последующие умозаключения.
Что такое суспензия
Суспензии (взвеси) – жидкие лекарственные формы, в которых твердые мелкораздробленные нерастворимые лекарственные вещества находятся во взвешенном состоянии в какой-либо жидкости.
Согласно Государственной Фармакопее
Суспензии – жидкая лекарственная форма, представляющая собой гетерогенную дисперсную систему, содержащую одно или несколько твердых действующих веществ, распределенных в жидкой дисперсионной среде.
Суспензии представляют собой дисперсные системы, состоящие из дисперсионной среды (вода, растительное масло, глицерин и т.п.) и дисперсной фазы (частицы твердых лекарственных веществ, практически нерастворимые в данной жидкости). Назначают суспензии для наружного и внутреннего употребления. Некоторые суспензии применяют парентерально. При этом надо иметь в виду, что суспензии следует вводить внутримышечно или в полости тела.
Чем меньше размер дисперсной фазы в суспензии, тем более (при прочих равных условиях) выражено ее терапевтическое действие. У суспензий, как и у других лекарственных форм, имеются свои преимуществ и недостатки. Они оказывают пролонгированное действие на организм. При назначении суспензий снижается отрицательное воздействие желудочного сока на лекарственные вещества, находящиеся в виде мелких частиц.
Преимущества суспензий
- более высокую дисперсность твердых веществ по сравнению с таблетками и порошками, что, в свою очередь, обеспечивает лучший терапевтический эффект;
- более быстрое проявление фармакологического действия (при размере час тиц менее 10 мкм) по сравнению с твердыми лекарственными формами;
- выраженное пролонгированное действие по сравнению с фармацевтическими растворами;
- удобство приема;
- возможность корригирования вкуса и запаха, что имеет существенное значение в педиатрической практике;
- возможность отпуска в виде сухого полуфабриката, который впоследствии суспендируют в воде непосредственно перед употреблением (это позволяет хранить действующие вещества достаточно длительное время).
Недостатком суспензий является возможность гидролитического разложения лекарственного вещества при длительном взаимодействии с дисперсионной (в основном водной) средой, что проявляется в процессе их хранения.
Пример суспензий
Лекарства-суспензии — Как правило, суспензии чаще всего встречаются в детских формах антибиотиков. Это Амоксиклав, Зиннат, Клацид, Супракс и другие препараты. Удобство индивидуального дозирования для детей, приятный вкус и длительный срок хранения антибиотиков в порошкообразном виде дают неоспоримые преимущества данным препаратам.

Вторыми по популярности лекарствами в форме суспензий являются противоязвенные/лекарства от изжоги. Пример лекарств — Эспумизан, Релцер, Мотилиум и Гевискон. Подобная лекарственная форма позволяет ускорить наступление терапевтического эффекта для данных лекарств.
Особенности суспензий
Одной из важнейших особенностей суспензий является их седиментационная (кинетическая) и агрегативная неустойчивость, которая определяет способы изготовления, хранения и приема данной лекарственной формы. Для обеспечения высокой эффективности препарата суспензии должны обладать высокой агрегативной устойчивостью — способностью противостоять укрупнению частиц и образованию агломератов, кинетической устойчивостью — способностью противостоять оседанию частиц и сохранять равномерное распределение частиц по всему объему суспензии, а также иметь низкую скорость седиментации.
Обычно частицы дисперсной фазы настолько велики (более 10 мкм), что оседают под действием силы тяжести (седиментируют). Суспензии, в которых седиментация идёт очень медленно из-за малой разницы в плотности дисперсной фазы и дисперсионной среды, иногда называют взвесями.
Что такое Эмульсия
Эмульсия – это жидкая лекарственная форма, в которой нерастворимые в воде жидкости (жирные масла, бальзамы) находятся в водной среде во взвешенном состоянии в виде мельчайших капель. Внешне эмульсии имеют сходство с молоком.
Согласно Государственной Фармакопее
Эмульсии – жидкие лекарственные формы, представляющие собой гетерогенную двухфазную дисперсную систему с жидкой дисперсной фазой и жидкой дисперсионной средой
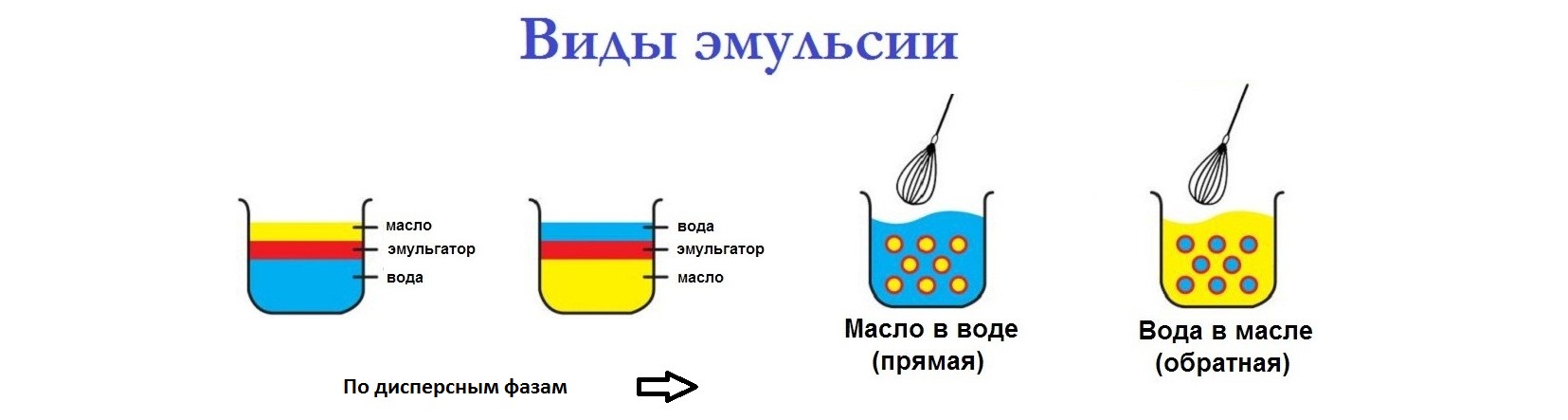
Простыми слова, опуская государственные определения , эмульсию проще всего представить и понять, как молоко. В случае с молоком это капли молочного жира, равномерно распределённые в воде. Если изучать более глубоко, то мы говорим о смеси трех веществ, два из которых — несмешивающиеся между собой жидкости, а третье — эмульгатор. Одна жидкость — это вода, вторая — молочный жир а эмульгатором выступает комплекс белка и лецитина.
Самое главное отличие эмульсий от суспензий и других лекарственных форм заключается в том, что Эмульсии могут быть типа масло/вода и вода/масло. Эмульсии могут расслаиваться, но при взбалтывании должны легко восстанавливаться. Для обеспечения устойчивости в состав эмульсий вводят эмульгаторы.
 Применение лекарственных веществ в виде эмульсий позволяет совмещать в одной лекарственной форме несмешивающиеся жидкости, маскировать неприятный вкус масел, смягчать раздражающее действие на слизистую оболочку некоторых лекарственных веществ, вводить в состав лекарства нерастворимые лекарственные вещества. Кроме того, масла в виде эмульсий лучше усваиваются в организме, так как всасывание масел в желудочно-кишечном тракте происходит только в присутствии ПАВ, способных их эмульгировать. К недостаткам эмульсий следует отнести их малую устойчивость, необходимость использования эмульгаторов и длительность приготовления.
Применение лекарственных веществ в виде эмульсий позволяет совмещать в одной лекарственной форме несмешивающиеся жидкости, маскировать неприятный вкус масел, смягчать раздражающее действие на слизистую оболочку некоторых лекарственных веществ, вводить в состав лекарства нерастворимые лекарственные вещества. Кроме того, масла в виде эмульсий лучше усваиваются в организме, так как всасывание масел в желудочно-кишечном тракте происходит только в присутствии ПАВ, способных их эмульгировать. К недостаткам эмульсий следует отнести их малую устойчивость, необходимость использования эмульгаторов и длительность приготовления.
По способу приготовления эмульсии подразделяют на масляные (Emulsa oleosa) и семенные (Emulsa seminalia).
Масляные эмульсии готовят из жидких масел: касторового (Oleum Ricini), миндального (Oleum Amygdalarum), рыбьего жира (Oleum jecoris) и др.
Чтобы из масла и воды образовалась эмульсия, необходимо эмульгировать масло, т.е. разделить его на мельчайшие капли. С этой целью масло смешивают со специальными веществами – эмульгаторами. В качестве эмульгаторов используют камеди, например камедь абрикосовую (Gummi Armeniacae), а также желатозу (Gelatosa).
Примеры эмульсий
Чаще всего эмульсии встречаются в лекарствах для наружного применения: бепантнен, фенистил, локойд и др; они равномерно наносятся на кожу, быстро всасываются, высыхают, не оставляют жирного блеска и не пачкают одежду.

Разница между эмульсиями и суспензиями
В этом разделе мы рассмотрим разницу между эмульсиям и суспензиями. Сказать правде в глаза, в случае эмульсий и суспензий тяжело заметить один и тот же препарат в разных лекарственных формах, поэтому сравнительный анализ затруднен и дальнейшее сравнение будет строиться на объективных факторах и свойствах этих лекарственных форм:
Суспензии | Эмульсии |
Достоинства | |
|
|
Недостатки | |
|
|
Примеры суспензий и эмульсий
Далее будут перечислены примеры лекарств суспензий и лекарств эмульсий:
Суспензии | Эмульсии |
|
|
Источник
